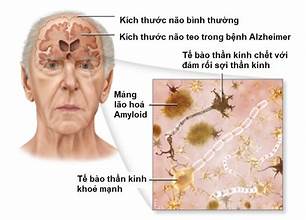
Alzheimer – Bệnh đa yếu tố và sự kết hợp các hợp chất thiên nhiên trong điều trị
Theo Liệu pháp điều trị bệnh Alzheimer, số đặc biệt, Wiley Online Library, 2020
Bệnh Alzheimer, một rối loạn thoái hóa thần kinh phức tạp gây ra nhiều thay đổi tế bào bao gồm suy giảm hệ thống cholinergic, kết hợp beta-amyloid (βA), tăng phosphoryl hóa tau, rối loạn cân bằng nội môi kim loại, viêm thần kinh và nhiều con đường khác có liên quan đến cơ chế bệnh sinh của bệnh.
Các sản phẩm tự nhiên như flavonoid, alkaloid, resveratrol và curcumin có đặc tính đa chức năng đã thu hút sự chú ý của các nhà nghiên cứu vì những phân tử này có khả năng tương tác đồng thời với nhiều mục tiêu đối với bệnh này. Do đó, các sản phẩm tự nhiên và các dẫn xuất của chúng với hiệu quả đã được chứng minh có thể được sử dụng trong việc điều trị các rối loạn thoái hóa thần kinh.
Các phối tử chỉ thị đa mục tiêu dựa trên sản phẩm tự nhiên bao gồm: tacrine-coumarin, tacrine-huperzine A, harmine-isoxazoline, berberine-thiophenyl, galantamine-indole, pyridoxine-resveratrol, donepezil-curcumin.
- Trị liệu bệnh Alzheimer hiện nay
Cho đến nay, không có liệu pháp điều trị hoặc phòng ngừa cho AD. Năm chất trung gian đã được Cục Quản lý Thực phẩm và Dược phẩm Hoa Kỳ (FDA) phê duyệt để quản lý AD gồm: tacrine, rivastigmine, donepezil và galantamine là chất ức chế acetylcholinesterase (AChEI), trong khi memantine là N-methyl-D-aspartate (NMDA) chất đối kháng thụ thể (Hình 1). Chất ức chế AChE đầu tiên được FDA chấp thuận là tacrine đã bị cấm do tác dụng độc gan của nó. Người ta nhận thấy rằng trong AD có sự giảm hoạt động của tế bào thần kinh cholinergic. Các chất ức chế acetylcholinesterase làm tăng nồng độ tiếp hợp của ACh bằng cách giảm tốc độ thủy phân ACh. Donepezil được chấp thuận để điều trị các giai đoạn nhẹ đến trung bình của AD. Hiện tại bệnh nhân AD đang được điều trị bằng thuốc ức chế AChEs và thuốc đối kháng NMDA giúp giảm bớt một số triệu chứng của AD.
Hình 1. Cấu trúc hóa học của thuốc được FDA chấp thuận cho AD. (a) Donepezil; (b) Galantamine; (c) Rivastigmine; (d) Tacrine; (e) Chất tạo màng
- Sản phẩm của tự nhiên
Các nghiên cứu dịch tễ học đã chỉ ra rằng việc hấp thụ một số thành phần trong chế độ ăn uống làm giảm nguy cơ AD, điều này khuyến khích một nhà nghiên cứu khám phá tác dụng của chiết xuất thực vật và cô lập các thành phần có hoạt tính. Mặt khác, một nghiên cứu toàn diện về các đặc tính hóa lý và dược liệu của các sản phẩm tự nhiên cho thấy rằng những sản phẩm này có các đặc tính giống như thuốc, có thể vượt qua màng sinh học và có khả năng can thiệp vào tương tác protein-protein. Các sản phẩm tự nhiên được coi là “chất chuyển hóa thứ cấp” của thực vật và thường có trọng lượng phân tử nhỏ hơn 3.000 Da. Một số hợp chất được phân lập từ các bộ phận khác nhau của cây như rễ, thân rễ, lá và hạt có khả năng ngăn chặn sự hình thành các mảng độc và tăng cường tín hiệu cholinergic. Chế độ ăn uống có đặc tính chống oxy hóa có khả năng giảm stress oxy hóa trong não.
2.1. Alcaloids
2.1.1. Galantamine
Galantamine là một alcaloid isoquinoline được phân lập từ hoa và củ của cây Galanthus caucasicus, Galanthus sworonowii, Leucojum aestivum, Lycoris radiate. Galantamine làm tăng mức ACh trong khe hở khớp thần kinh bằng cách ức chế cạnh tranh AChE và cũng hoạt động như một chất điều biến dị ứng của thụ thể nicotinic acetylcholine (nAChRs). Một số dẫn xuất của galantamine được tổng hợp bằng cách liên kết chúng với memantine bằng các liên kết có độ dài và thành phần khác nhau. Chúng được đánh giá là chất ức chế AChE, chất kết dính NMDAR, và cũng cho tính chọn lọc đối với tiểu đơn vị 2B (NR2B) của NMDAR.
Người ta thấy rằng dẫn xuất 1a ức chế AChE với IC50 là 0,52 nM. Dẫn xuất 1b hoạt động như một chất đối kháng NMDAR với giá trị Ki là 2,32 μM và cũng ức chế AChE với IC50 là 695,9 nM. Dẫn xuất 1c cho thấy ái lực liên kết với NR2B (Ki là 2,9 μM) với hoạt tính bảo vệ thần kinh.
Thêm vào đó, lai liên kết vị trí kép mới của gốc galantamine và indole được tổng hợp và gắn vào rhAChE. Các dẫn xuất 1d – f cho thấy hoạt tính ức chế AChE cao nhất với các giá trị IC50 tương ứng là 0,011 μM, 0,012 μM và 0,015 μM (Hình 2).
Trong các dẫn xuất galantamine-indole, gốc galantamine tương tác với CAS và phần indole liên kết với các gốc thơm ở vị trí anion ngoại vi và các dẫn xuất này hoạt động như chất kết dính vị trí kép với enzyme rhAChE.
Hình 2. Các phân tử dựa trên Galantamine cho AD
2.1.2. Huperzines
Huperzine A và B là các alkaloid lycopodium được chiết xuất từ Huperiza serrata. Cây thuốc dân gian Trung Quốc này được sử dụng để điều trị sưng tấy, lú lẫn, tâm thần phân liệt, sốt và căng thẳng. Huperzine A là chất ức chế cụ thể, mạnh và có thể đảo ngược của AChE và BuChE với IC50 là 0,82 nM và 74,43 nM (Bảng 1, 2a). Huperzine B cũng là một chất ức chế có thể đảo ngược AChE với IC50 của 14,3 μM (Bảng 1, 2b) và cho thấy hiệu quả cao hơn. Do đó, Huperzine A và B được sử dụng rộng rãi như động lực tự nhiên để thiết kế các AChEI mạnh hơn. Các chất ức chế AChE liên kết chặt mới lạ bao gồm cấu trúc phụ carbo-bicyclo của Huperzine A và cấu trúc phụ 4-aminoquinoline (từ tacrine) với các nhóm thế khác nhau đã được đề xuất là chất ức chế AChE đầy hứa hẹn (Bảng 1, 2c và 2d).
Tacrine – Huperzine A lai (Huprines) mạnh hơn (-)- huperzine A và tacrine đơn thuần (lên tới 13 lần và 25 lần). Trong số các dẫn xuất được thay thế, các dẫn xuất hoạt động nhất chứa clo ở vị trí 3 và 9 với nhóm metyl hoặc etyl. Một loạt các dị phân tử bao gồm dimethoxyindanone của donepezil và pyridone của huperzine A được liên kết với nhau bởi độ dài khác nhau của liên kết methylene đã được báo cáo là chất ức chế AChE đầy hứa hẹn. Hợp chất 2e với liên kết tetramethylene được tìm thấy là chất ức chế AChE mạnh nhất với IC50 là 9 nM. Huperzine A và các dẫn xuất imine (các hợp chất trong Bảng 1 2f, 2g, 2h và 2i) với vòng thơm nhỏ được thay thế bổ sung cho thấy sự ức chế hAChE hiệu quả trong phạm vi nano. Vòng thơm của dẫn xuất Huperzine A thể hiện sự xếp π-π với gốc amino axit là AChE. Các dẫn xuất 2f, 2g, 2h và 2i hoạt động mạnh hơn xấp xỉ 865 lần, 1,065 lần, 477 lần, và 517 lần so với chất mẹ Huperzine A.
Bảng 1. Huperzine A, B có nguồn gốc tự nhiên và các dẫn xuất của chúng ức chế cholinesterase
| Hợp chất | Cấu trúc | R và X | IC50 (nM) | ||
| hAChE | hBuChE | TcAChE | |||
| 2a. (-)-Huperzine A | – | 0,82 | 74,43 | 11,4 | |
| 2b. Huperzin B | – | 14,3 | 214,0 | – | |
| 2c. rac – 2c | R – CH3 | 0,78 ± 0,02 | 236 ± 44 | – | |
| (-)- 2c | 0,03 ± 0,1 | 247 ± 18 | – | ||
| (+)- 2c | 23 ± 18 | 153 ± 31 | – | ||
| 2d. rac – 2d | R – CH2CH3 | 0,75 ± 0,06 | 15,8 ± 2,4 | – | |
| (-)- 2d | 0,32 ± 0,09 | 159 ± 10 | |||
| (+)- 2d | 23,1 ± 2,3 | 58,3 ± 5,9 | – | ||
| 2e. (RS, S) | – | 9 ± 1 | – | – | |
| 2f | R1, R2, R4 – H
R3 – OCH3 |
31 | – | 0,0246 | |
| 2g | R1, R3 – H
R2, R4 – OCH3 |
29 | – | 0,02 | |
| 2h | R2, R4 – H
R1, R3 – OCH3 |
84 | – | 0,0446 | |
| 2i | R1, R2, R4 – H
R3 – CN |
22 | – | 0,0412 | |
| 2j | R – F
X – CH |
– | – | 29,7 | |
| 2k | R – H
X – N |
– | – | 10,5 | |
| 2l | – | – | – | 4,93 ± 0,23 | |
| 2m | – | 2,39 | 513 | – | |
Các dẫn xuất mới của Huperzine B được thiết kế hợp lý, trong đó 16 vị trí của nhóm Huperzine B được kết nối thông qua một chuỗi tether với vòng thơm ở cuối, hỗ trợ tác động qua lại với PAS. Các dẫn xuất 2j và 2k là chất ức chế AChE mạnh hơn (480 đến 1.360 lần) và cũng là chất ức chế BuChE mạnh (370 đến 1.560 lần) so với Huperzine B gốc. Ngoài ra, hợp chất 2k cũng có đặc tính bảo vệ thần kinh chống lại độc tính tế bào do H2O2 gây ra trong tế bào PC12. Dẫn xuất mới bis-huperzine B liên kết vị trí kép 2l, được phát hiện là chất ức chế AChE mạnh nhất (3.900 lần) so với huperzine B. Trong hợp chất 2l, liên kết dài chứa hai nguyên tử nitơ tích điện dương có thể tác động lẫn nhau qua liên kết hydro hoặc tương tác cation-π với vị trí hoạt động của AchE. Các chất lai đa mục tiêu mới của rhein-huprin đã được thiết kế, trong đó hệ thống hydroxyanthraquinone được gắn vào thông qua các trình liên kết đa dạng với một đơn vị huprin Y. Huprin Y tương tác với CAS trong khi các vòng thơm của rhein tạo ra tương tác xếp chồng π-π với PAS của AChE do đó hoạt động như một chất ức chế hai vị trí. Trong số các dẫn xuất được thay thế, hợp chất 2m thể hiện hoạt tính ức chế mạnh đối với hAChE, hBuChE, BACE-1 (với các giá trị IC50 tương ứng là 2,39 nM, 513 nM, 80 nM) cùng với 43% ức chế sự tập hợp Aβ42 ở 10 μM, do đó, hợp chất 2m có thể là một hứa hẹn thay đổi ứng cử viên thuốc chống Alzheimer.
2.1.3 Berberine
Berberine là một alkaloid benzylisoquinoline thường được tìm thấy trong rễ, thân rễ, thân và vỏ của các loại cây như Berberis spp., Coptis chinensis, Hydrastis canadensis, và Phellodendron amurense. Nó có tác dụng chống oxy hóa, chống viêm, kháng u và kháng khuẩn mạnh, cùng với các đặc tính bảo vệ tim mạch và thần kinh. Berberine ức chế cả AChE (IC50 là 0,37) và BuChE (IC50 là 18,21 μM), nhưng chọn lọc hơn đối với AChE. Ngoài ra, berberine có hoạt tính đối kháng với thụ thể NMDA (đặc biệt là NR1) và cũng chặn dòng điện kali phụ thuộc vào điện thế, dẫn đến bảo vệ thần kinh. Do đó, berberine giúp tăng cường kích thích cholinergic và cải thiện tình trạng suy giảm nhận thức ở AD. Các dẫn xuất liên kết vị trí kép mới của gốc triazole và berberine được tổng hợp và gắn vào TcAChE (Torpedo californica acetylcholinesterase). Dẫn xuất 3c, trong đó vị trí 4 của vòng triazole được thay thế bằng diisopropylamino, ức chế AChE với IC50 là 0,044 μM. Trong dẫn xuất 3d, vị trí 4 của vòng triazole được thay thế bằng butyl ức chế 79% sự kết hợp βA ở 20 μM.
Hơn nữa, các chất lai berberine-thiophenyl được tổng hợp trong đó oxy hoặc nhóm NH của các dẫn xuất berberine được thay thế bằng một nguyên tử lưu huỳnh, dẫn đến tăng cường các đặc tính chống oxy hóa. Trong số các dẫn xuất, hợp chất 3a berberine được ghép với o-methylthiophenyl bằng chất đệm ethylene và được phát hiện là chất ức chế mạnh AChE (IC50 là 0,077) hơn BuChE (IC50 = 1.360 μM). Dẫn xuất 3b của berberin với o-chlorothiophenyl được tìm thấy không chỉ là chất ức chế AChE mạnh (IC50 là 0,042 μM) mà còn là chất ức chế BuChE mạnh (IC50 là 0,662) (Hình 3). Các dẫn xuất mới này cũng ức chế sự kết hợp βA và có đặc tính chống oxy hóa.
Hình 3. Thiết kế đa phân tử dựa trên Berberine cho AD
2.1.4. Harmine
Harmine thuộc họ β-carboline alkaloid, được phân lập từ cây nho Nam Mỹ Banisteriopsis caapi và có cấu trúc bao gồm lõi indole và pyridine. Harmine có đặc tính chống nấm, kháng khuẩn, chống tái tạo mô, chống oxy hóa và chất ức chế DYRK1A. Ngoài ra, Harmine 4a cũng là một chất ức chế mạnh hơn quá trình tăng phosphoryl hóa protein tau và cũng ức chế quá trình phosphoryl hóa trực tiếp được xúc tác bởi DYRK1A của tau tại Ser396 với IC50 là 700 nM. Thêm vào đó, harmol 4b và 9-ethylharmine 4c cho giá trị IC50 được cải thiện lần lượt là 90 nM và 400 nM. Harmine ức chế AChE với IC50 là 9,0 μM.. Một loạt các dẫn xuất harmine-isoxazoline đã được tổng hợp, trong đó dẫn xuất được thế phenyl 4d có hoạt tính ức chế AChE tốt nhưng nó kém mạnh hơn harmine 4a (Hình 4).
Hình 4. Các phân tử đa chức năng biến đổi của Harmine
2.1.5. Aporphine alkaloids
Aporphine alkaloids có cấu trúc phụ là tetrahydroisoquinolin và thuộc nhóm alkaloid isoquinolin. Chúng được phân lập từ thân rễ của cây Menispermum dauricum. Aporphin alkaloid, chẳng hạn như oxoisoaporphine và oxoaporphine có các đặc tính sinh học đa dạng, ví dụ như ức chế telomerase cholinesterase và sự kết hợp βA cùng với khả năng chống oxy hóa, điều hòa miễn dịch và hoạt động chống khối u. Vị trí của nguyên tử nitơ trong dược chất chỉ phân biệt giữa oxoaporphine và oxoisoaporphine alkaloid, oxoaporphine thường được gọi là 1-azabenzanthrone trong khi oxoisoaporphine được gọi là 6-azabenzanthrone. Các dẫn xuất oxoisoaporphine tổng hợp là chất ức chế AChE mạnh (5a, 5b với IC50 là 4,8 × 10-4 ± 0,8 ở 10-4 μM và 2,62 × 10-3 ± 0,2 ở 10-3 μM). Các dẫn xuất oxoaporphine tổng hợp 5c và 5d (IC50 tương ứng là 0,35 μM và 0,11 μM) là chất ức chế AChE mạnh hơn gấp hai đến ba lần so với dẫn xuất oxoisoaporphine. Nghiên cứu mô hình phân tử mô tả rằng phân tử 1-azabenzanthrone của các alcaloid oxoisoaporphine có thể liên kết với phần dư Trp279 của PAS của AChE bằng tương tác xếp chồng π-π. Khả năng hòa tan trong nước và tính chọn lọc của oxoisoaporphine alkaloid đối với AChE đã được cải thiện đáng kể bằng cách đưa các amin hoặc nhóm amoni làm chất đệm. Một loạt dẫn xuất mới của oxoisoaporphine-tacrine được kết nối thông qua một amino alkyl tether đã được tổng hợp. Trong số các dẫn xuất mới, 5e được tìm thấy ức chế eeAChE mạnh hơn 31 lần (IC50 = 3,4 nM) so với tacrine và cũng cho thấy hoạt động chống lại EqBuChE với IC50 là 110 nM. Tất cả các dẫn xuất mới thể hiện hoạt tính chống phân ly βA; chất ức chế mạnh sự kết hợp βA tự gây ra ở 10 μM (35,5 – 85,8%) và cũng ức chế sự kết hợp βA do AChE gây ra ở 100 μM.
Một loạt các dẫn xuất oxoisoaporphine liên kết với một chuỗi bên cơ bản đa dạng ở vị trí 9 được tổng hợp và đánh giá về khả năng ức chế AChE, tất cả các dẫn xuất đều cho thấy giá trị IC50 trong phạm vi nano. Hợp chất 5f với pyrrolidine làm chuỗi bên cơ bản, thể hiện khả năng ức chế AChE mạnh (IC50 là 1,06 nM) và cũng có tỷ lệ chọn lọc cao nhất (1,850 lần). Các hợp chất cation tổng hợp 5f và 5g với nitơ bậc bốn làm chuỗi bên cơ bản cho thấy hoạt tính ức chế AChE cao hơn tương ứng ở 1,06 nM và 1,08 nM, so với các hợp chất nitơ bậc bốn tương ứng là 5h và 5i với tác dụng ức chế AChE là 6,18 nM và 2,47 nM (Hình 5).
Yang và cộng sự (2012) đã báo cáo việc phân lập các alkaloid aporphin, cụ thể là N-methylasimilobine, nuciferine và nornuciferine từ Nelumbo nucifera và thử nghiệm sự ức chế AChE. N-methylasimilobine cho thấy ức chế 50% AChE ở nồng độ 1,5 ± 0,2 μg/ml ở chế độ thuận nghịch và không cạnh tranh. Tám dẫn xuất của nuciferine được tổng hợp bằng phản ứng dealkyl hóa (ở oxy và nitơ) và phản ứng thơm hóa vòng. Các dẫn xuất 1,2-Dihydroxyaporphine và dehydronuciferine ức chế AChE với IC50 tương ứng là 28 và 25 μg/ml.
Hình 5. Cấu trúc thay đổi của aporphin alkaloid
- Flavonoids
Flavonoid là một nhóm các chất dinh dưỡng thực vật polyphenolic được tìm thấy trong hầu hết các loại trái cây, hoa, hạt và rau. Chúng phổ biến hơn ở thực vật bậc cao có nhiều trong các họ như Polygonaceae, Rutaceae, Leguminosae, Umbelliferae và Compositae. Do bản chất polyphenol, chúng có khả năng quét các gốc tự do, hydrogen peroxide và gốc superoxide và do đó có khả năng bảo vệ thần kinh. Đặc tính thu dọn gốc tự do của polyphenol thay đổi theo số lượng và vị trí của các nhóm hydroxyl. Bảng 2 bao gồm ảnh hưởng của polyphenol đối với các yếu tố gây bệnh AD khác nhau. Do đó, một loạt các dẫn xuất flavonoid mới đã được phát triển vì đặc tính chống oxy hóa của chúng.
Flavonoid có thể được chia thành nhiều nhóm phụ khác nhau tùy thuộc vào vị trí của vòng B trên cacbon của vòng C và mức độ không bão hòa và oxy hóa của vòng C. Isoflavone là những hợp chất trong đó vòng B được gắn ở vị trí 3 của vòng C, có cấu trúc 3-phenylchromen-4-one. Trong trường hợp của neoflavonoid, vòng B được gắn ở vị trí 4 của vòng C, tức là cấu trúc 4-phenylcoumarine. Trong trường hợp có các phân nhóm sau: flavon, flavo-nols, flavanones, flavan-3-ol hoặc flavanols hoặc catechin và chalcones, thì vòng B được gắn vào vị trí 2 của vòng C; chỉ khác nhau về đặc điểm cấu trúc của vòng C (Hình 6).
Bảng 2. Ảnh hưởng của polyphenol trên các con đường bệnh lý khác nhau liên quan đến AD
| Lớp polyphenol | Ví dụ và nguồn gốc | Ảnh hưởng đến AD |
| Phenolic acids | Gallic acid (trà, đinh hương, nho, dâu tây) | Ngăn chặn việc sản xuất βA trong AD chuột bằng chống oxy hóa và cải thiện nhận thức ở chuột AD, ngăn chặn quá trình apoptosis |
| Caffeic acid (trà, cà phê, rượu vang đỏ, vỏ cây bạch đàn) | Ức chế sự kết hợp AChE và βA; cải thiện tình trạng thiếu trí nhớ ở mô hình chuột bằng cách tăng cường hoạt động của choline acetyltransferase (CAT) và superoxide dismutase (SOD); thúc đẩy hoạt động chống oxy hóa bằng cách ức chế quá trình peroxy hóa lipid. Ức chế sản xuất oxit nitric. | |
| Curcumin (nghệ) | Ức chế quá trình peroxy hóa lipid và AChE, tăng cường nhận thức, GSH và protein axit dạng sợi thần kinh đệm (GFAP) và ức chế sự kết hợp βA trên mô hình chuột; điều chỉnh thụ thể NMDA. | |
| Flavones | Apigenin (cần tây) | Ức chế tín hiệu MAPK trong dòng tế bào u nguyên bào thần kinh “SH-SY5Y”. Ngăn chặn stress oxy hóa và ức chế sự tự kết hợp βA và Cu2+. Cải thiện khả năng học tập và trí nhớ ở chuột AD chuyển gen kép APP / PS1 |
| Luteolin (cần tây, cỏ xạ hương, ớt xanh và trà hoa cúc) | Ức chế ChE’s và β-secretase, ngăn chặn sự hình thành βA và điều chỉnh sự biểu hiện của APP. Làm giảm sự tập hợp Aβ, tăng phosphoryl hóa tau, chất trung gian gây viêm, kích hoạt GSK-3, ngăn chặn quá trình chết rụng tế bào thần kinh bằng cách giảm sự tạo ROS nội bào, tăng hoạt động của SOD | |
| Isoflavones | Genistein (đậu nành) | Ức chế các con đường truyền tín hiệu NF-κB, JNK và ERK ở chuột để chống lại tổn thương tế bào do H2O2 gây ra. Ức chế sự tổng hợp βA |
| Flavonols | Quercetin (trà, hành, táo, quả mọng) | Ức chế sự tập hợp βA, quá trình tăng phosphoryl hóa tau, làm tăng hoạt động của protein kinase được kích hoạt bởi adenosine monophosphate, dẫn đến tăng cường nhận thức ở mô hình chuột AD chuyển gen. Loại bỏ ROS và tăng cường hoạt động SOD biểu thị hoạt động chống oxy hóa |
| Kampferol (trà, tỏi tây, cà chua) | Ở chuột, ức chế mảng βA và đảo ngược βA gây ra suy giảm hiệu suất | |
| Flavanones | Naringenin (Rau má – Centella asiatica, trái cây họ cam quýt) | Hoạt tính ức chế AChE, ngăn ngừa độc tính βA và hoạt tính chống oxy hóa |
| Chalcones | Butein (cây sơn mài Trung Quốc – Chinese lacquer tree) | Ức chế các chất trung gian gây viêm thần kinh và tăng cường GSH do đó cung cấp sự bảo vệ thần kinh chống lại stress oxy hóa |
| Phloridzin (táo) | Gây ra hoạt động loại bỏ ROS và tăng cường SOD | |
| Flavanols (monomer) | Catechin, Epicatechin, Gallocatechin, Epigallocatechin gallate (sô cô la, mướp đắng, trà xanh) | Hoạt động chống oxy hóa, tăng cường trí nhớ, chelator kim loại, có các hoạt động chống viêm và chống phân mảng bằng cách tăng α-secretase, giảm β và γ-secretase |
| Stilbenes | Resveratrol và Piceatannol (rượu vang đỏ, raps, đậu phộng và nam việt quất) | Ở chuột cảm ứng βA25-35 cải thiện đáng kể nhận thức đồng thời tăng ChAT, đặc tính chống oxy hóa, ức chế sự kết hợp βA, giảm độc tính và ức chế quá trình chết rụng tế bào. |
| Flavanols (polymer) | Tannic acid, Proanthocyanidins (hồng, quế, nho, việt quất, nho đen) | Ức chế stress oxy hóa; ức chế kết tập tau; tăng cường học tập và nhận thức ở chuột |
Hình 6. Phân loại flavonoid và cấu trúc hóa học
3.1. Flavones
Flavone chủ yếu hiện diện trong lá, hoa và quả, có tác dụng ức chế các sản phẩm cuối quá trình glycation nâng cao (AGEs), chống viêm, chống oxy hóa và bảo vệ thần kinh. Hình 7 cho thấy một vài dẫn xuất dựa trên khung phân tử flavon.
3.2. Isoflavones
Isoflavonoid thường được tìm thấy trong các cây họ đậu, như đậu nành, và được phân lập từ vi sinh vật. Chúng hoạt động như tiền chất để tổng hợp phytoalexin trong quá trình tương tác giữa thực vật và vi sinh vật. Một loạt các chất tương tự isoflavone đã được đánh giá về các hoạt động ức chế của chúng đối với AChE và MAO-B (Hình 7).
Hình 7. Thiết kế các phân tử đa chức năng dựa trên khung phân tử của (a) flavon; (b) isoflavone; (c) flavanones
3.3. Flavanones
Flavanones (ví dụ, hesperetin) là một phân nhóm quan trọng khác của flavonoid được tìm thấy trong tất cả các loại trái cây họ cam quýt như cam, chanh và nho. Chúng có đặc tính loại bỏ gốc tự do và cũng có đặc tính chống viêm, giảm lipid máu và giảm cholesterol. Do đó, việc sử dụng flavanones để tổng hợp MTDL đã được thực hiện.
3.4. Chalcones
Chalcones là một trong những phân nhóm của flavonoid, được gọi là flavonoid chuỗi mở vì không có vòng C của cấu trúc khung flavonoid cơ bản (Hình 6). Chúng có mặt với số lượng lớn trong cà chua, lê, dâu tây, quả mâm xôi và một số sản phẩm lúa mì. Chalcones và các dẫn xuất của chúng (Hình 8) đã tạo ra sự đánh giá cao của các nhà nghiên cứu như tác nhân chống bệnh Alzheimer vì số lượng lớn các lợi ích sinh học mà chúng mang lại.
Hình 8. Các phân tử đa chức năng dựa trên chalcones
3.5. Neoflavonoids
Neoflavonoid được đặc trưng bởi sự hiện diện của nhóm keto ở vị trí 2 và nhóm phenyl ở vị trí 4 của vòng C (Hình 6). Coumarin là một neoflavonoid chủ yếu được tìm thấy trong nhiều loại thực vật và có một loạt các hoạt động sinh học. Các nghiên cứu mô hình phân tử cho thấy rằng nó liên kết với PAS của AChE và hoạt động như một chất ức chế mạnh mẽ AChE và cũng ức chế sự kết hợp βA. Một loạt phép lai mới của tacrine-coumarin được báo cáo trong đó cả hai giá thể được liên kết bởi một chất đệm alkyl dựa trên piperazine (Hình 9).
Hình 9. Phối tử hướng đa mục tiêu (MTDL) dựa trên Coumarin
Dẫn xuất 10a có hoạt tính ức chế mạnh đối với EeAChE (IC50 là 0,092 μM) và trung bình đối với EqBuChE (IC50 là 0,234 μM), đặc tính chống kết tụ βA (ức chế 67,8% ở 20 μM) và cũng có khả năng chelat kim loại Cu2+ và Fe2+ do amide của nó liên kết. Hơn nữa, gốc coumarin liên kết với thiourea, (hợp chất 10b) được tìm thấy là chất ức chế AChE mạnh nhất với giá trị IC50 là 0,04 μM. Trong các dẫn xuất MTDL dựa trên coumarin (10c và 10d), vị trí 6 và 7 của coumarin được liên kết với chất đệm alkyl có độ dài khác nhau với nhóm amin dietyl đầu cuối dẫn đến ức chế AChE của con người ở nồng độ nano (IC50 lần lượt là 11,7 nM và 12,9 nM) cùng với hoạt tính ức chế đáng kể đối với sự tự kết hợp βA42 khoảng 60% và hoạt động bảo vệ thần kinh đầy hứa hẹn, điều này làm cho hợp chất này trở thành một tác nhân điều chỉnh bệnh tiềm năng.
Khi coumarin được gắn vào gốc dithiocarbamate, thì hợp chất 10e cho thấy hoạt động ức chế tốt nhất đối với hAChE (IC50 là 0,027 μM) và cũng hoạt động như một chất chống đông máu βA (40,19% ở 25 μM).
Các nghiên cứu mô hình động học và phân tử cho thấy rằng hợp chất 10e là một chất ức chế hỗn hợp; chỉ ra rằng nó có thể tương tác với CAS cũng như PAS của AChE. Nghiên cứu chelation kim loại cho thấy dẫn xuất 10e chelate ion Fe3+ một cách chọn lọc. Hơn nữa, các dẫn xuất mới của gốc N-benzyl pyridinium với coumarin được tổng hợp trong đó hợp chất 10f cho thấy hoạt tính ức chế mạnh đối với eeAChE (IC50 giá trị 37,3 nM), một chất ức chế chọn lọc và cạnh tranh của hMAO-B (IC50 giá trị 1,57 μM) và chất ức chế mạnh tổng hợp βA (62,1% ở 20 μM).
Các nghiên cứu mô hình động học và phân tử cho thấy rằng dẫn xuất 10f là một chất ức chế kiểu hỗn hợp tương tác đồng thời với CAS và PAS của AchE. Tương tự, gốc N-benzylpiperidine của donepezil đã được báo cáo kết hợp với coumarin với độ dài khác nhau của miếng đệm. Hợp chất 10g cho thấy hoạt tính ức chế mạnh đối với hAChE (giá trị IC50 1,37 μM) và ức chế chọn lọc hMAO-B (IC50 = 2,62 μM) và cũng không độc đối với tế bào u nguyên bào thần kinh SH-SY5Y. Coumarin-pargyline hybrid 10h ức chế chọn lọc hMAO-B (giá trị IC50 0,27 μM) và là chất ức chế trung bình sự kết hợp βA (54% ở 25 μM) và gây độc tính thấp cho tế bào PC12. Một loạt kiểu lai coumarin-thiazole mới được tổng hợp trong đó trình tự liên kết giữa chuỗi N-alkyl và lõi dị vòng là gốc acetamide. Trong số này, hợp chất 10i là một chất ức chế hỗn hợp mạnh của AChE (IC50 = 43 nM).
- Resveratrol
Resveratrol (3,5,40-trihydroxystilbene) là một loại polyphenol tự nhiên chủ yếu được tìm thấy trong thực phẩm như đậu phộng, nho, rượu vang đỏ, quả mọng và có các hoạt tính sinh học đa dạng như đặc tính chống ung thư, chống viêm và bảo vệ thần kinh. Resveratrol là một tác nhân chống AD do chất chống oxy hóa, ức chế chống phân ly và loại triệt để βA.
Cấu trúc stilbene của hợp chất chịu trách nhiệm cho hoạt động ức chế MAO của nó. Gần đây, một loạt các dẫn xuất pyridoxine-resveratrol (Hình 10) đã được thành lập như chất ức chế mạnh cholinesterase và cũng hoạt động như một chất chống oxy hóa và có đặc tính chelat hóa kim loại. Các hợp chất 11a và 11b có nhóm thế piperidin (11a) và dietylamin (11b), hoạt động như chất ức chế AChE mạnh với giá trị IC50 tương ứng là 2,11 μM và 1,56 μM. Dẫn xuất 11c có nhóm thế morpholine hoạt động như một chất ức chế MAO-B mạnh với giá trị IC50 là 2,68 μM. Tất cả các dẫn xuất đều thể hiện hoạt tính chống oxy hóa tốt với các giá trị từ 1,52 – 2,63 của Trolox eq * ở 50 μM. Hợp chất 6c trong đó 3-và 4-hydroxy không tự do, được bảo vệ bằng isopropylidene, là chất chống oxy hóa yếu hơn so với hợp chất 11a và 11b. Điều này cho thấy rằng các nhóm hydroxy tự do có thể đóng góp vào hoạt động chống oxy hóa.
Hình 10. Các phân tử đa chức năng được thiết kế dựa trên khung phân tử của resveratrol
- Curcumin
Curcumin được phân lập từ cây Curcuma longa (nghệ) và thuộc họ Zingiberaceae. Về mặt hóa học, chất curcumin là một diarylheptanoid, còn được gọi là diferuloylmethane. Về mặt cấu trúc, curcumin là một hợp chất cacbonyl không no α, β với vòng thơm phẳng gắn liền. Nó có một loạt các hoạt động dược lý bao gồm chống viêm, chống ung thư, kháng khuẩn, chống oxy hóa và tác dụng chữa lành vết thương. Nó cũng thể hiện hoạt động chống lại các bệnh thần kinh bao gồm AD, bệnh Parkinson, bệnh đa xơ cứng, động kinh, tâm thần phân liệt và trầm cảm. Curcumin có khả năng ức chế sự kết hợp βA.
Do các hoạt tính dược lý đa dạng của nó, các chất tương tự curcumin khác nhau (Hình 11) đã được tổng hợp và đánh giá. Các chất tương tự curcumin thể hiện các hoạt động chống lại sự kết hợp AChE, Tau, βA1-42, enzyme phân cắt β-secretase (BACE1) và một số trong số chúng có khả năng quét các gốc tự do và cũng có thể che giấu các ion kim loại.
Lời kết
Bệnh Alzheimer là một vấn đề sức khỏe lớn của người cao tuổi và nhiều báo cáo chỉ ra rằng số lượng dân số bị ảnh hưởng sẽ tăng lên trong những năm tới. Phác đồ dùng thuốc hiện nay không có tác dụng chữa khỏi bệnh. Nhiều hợp chất tự nhiên đơn lẻ và sự kết hợp của chúng với các loại thuốc khác được sử dụng ở bệnh nhân AD để cải thiện trí nhớ và nhận thức. Những hạn chế chính liên quan đến các sản phẩm tự nhiên là sinh khả dụng thấp và ít hiệu quả lâm sàng, hạn chế việc phân phối thuốc đến mục tiêu để phát huy tác dụng dược lý của chúng. Do đó, các nỗ lực đã được thực hiện để thiết kế các phân tử mới dựa trên các bản chất tự nhiên, đặc biệt để phát triển phối tử hướng đa mục tiêu để chống lại bệnh đa yếu tố và loại bỏ các nhược điểm của các sản phẩm tự nhiên vốn là nhu cầu của quá trình phát triển thuốc hiện nay.
Nghiên cứu cho thấy rằng các sản phẩm tự nhiên như curcumin, resveratrol, alkaloids, flavonoid và các dẫn xuất của chúng có thể hữu ích trong việc làm giảm các triệu chứng của AD. Do tính chất đa yếu tố của bệnh, các phân tử đã được thiết kế trên chiến lược đa mục tiêu. Do đó, các phân tử có khả năng điều chỉnh nhiều mục tiêu như acetylcholinesterase, tập hợp βA, tăng phosphoryl hóa tau, rối loạn cân bằng nội môi kim loại, stress oxy hóa, và nhiều phân tử khác là cần thiết để làm chậm sự tiến triển của bệnh hoặc có khả năng chữa khỏi AD.