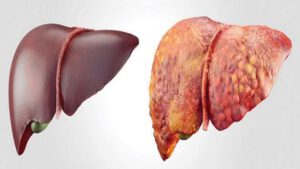
Lời bạt: cách đây 50 năm các tác giả hiểu về xơ gan đã đúng nhưng còn rất sơ sài, do vậy hiệu quả điều trị xơ gan chưa được cao. Cùng với sự phát triển khoa học chung, ngày nay, những hiểu biết mới ở cấp độ sinh học phân tử đa giúp các bác sĩ dần làm chủ trong chẩn đoán, điều trị, tiên lượng và xử trí. Bài này do Bác sĩ Hoàng Đôn Hoà biên soạn/biên tập có thể là dịp các bác sĩ có tuổi cập nhật mới và các Bác sĩ trẻ ôn lại kiến thức – hy vọng có lợi ích cho người làm chuyên môn và cộng đồng thụ hưởng.
Bác sĩ Hoàng Sầm
PHẦN I: GIẢI PHẪU HỌC CỦA GAN – CẤU TRÚC CƠ BẢN, VI MÔ VÀ TUẦN HOÀN MÁU
I.1. VỊ TRÍ – HÌNH THỂ NGOÀI – PHÂN THÙY GIẢI PHẪU
1.1.1. Vị trí và hình thể
Gan là cơ quan nội tạng lớn nhất cơ thể, chiếm khoảng 2–3% trọng lượng cơ thể ở người lớn (~1,4–1,8 kg).
Nằm ở hạ sườn phải, dưới cơ hoành, một phần vượt qua đường giữa sang hạ sườn trái.
Gan có hình nón cụt ngược hoặc hình lăng trụ tam giác, đáy nằm sát vòm hoành, đỉnh hướng về rốn.
1.1.2. Mặt ngoài
Mặt hoành: trơn, lồi, áp sát cơ hoành; có hố ấn tim, ấn phổi phải.
Mặt tạng (mặt dưới): lõm, tiếp xúc với dạ dày, tá tràng, thận phải, tuyến thượng thận và đại tràng ngang.
Có 2 thùy lớn theo giải phẫu học kinh điển: phải – trái, ngăn cách bởi dây chằng liềm.
1.1.3. Thùy theo chức năng
Theo phân thùy Couinaud – dựa trên sự phân bố tĩnh mạch cửa – gan chia thành 8 phân thùy chức năng, mỗi thùy có mạch máu riêng:
+ Thùy I: thùy đuôi (caudate)
+ Thùy II – IV: thuộc gan trái
+ Thùy V – VIII: thuộc gan phải
Cấu trúc này cực kỳ quan trọng trong chẩn đoán hình ảnh và phẫu thuật (cắt gan theo thùy chức năng).
I.2. HỆ MẠCH MÁU CỦA GAN – TUẦN HOÀN NGOẠI VÀ NỘI SINUSOID
1.2.1. Tuần hoàn kép
Gan là cơ quan có hệ tuần hoàn độc đáo nhất: có 2 nguồn máu vào và 1 đường máu ra:
| Loại mạch | Tên | Tỷ lệ cung cấp máu | Chức năng |
|---|---|---|---|
| Động mạch | Động mạch gan riêng (hepatic artery proper) | 25–30% | Giàu oxy |
| Tĩnh mạch | Tĩnh mạch cửa (portal vein) | 70–75% | Giàu chất dinh dưỡng từ ống tiêu hoá |
| Tĩnh mạch gan | 3–4 nhánh → tĩnh mạch chủ dưới | 100% | Dẫn máu ra khỏi gan |
Tĩnh mạch cửa: dẫn máu từ dạ dày, ruột, tụy, lách tới gan → giàu chất hấp thu và độc chất cần chuyển hoá.
Động mạch gan: nhánh của thân tạng (celiac trunk), dẫn oxy đến nhu mô gan.
1.2.2. Vi tuần hoàn trong gan – Sinusoid
Máu từ động mạch và tĩnh mạch cửa nhập vào mao mạch xoang (sinusoids) – mạch máu đặc biệt có thành mỏng, không liên tục, nhiều cửa sổ (fenestrations).
Các tế bào nội mô không có màng đáy → cho phép trao đổi nhanh các chất giữa máu – tế bào gan.
Trong sinusoid có:
+ Tế bào Kupffer: đại thực bào cố định → lọc vi khuẩn, hồng cầu chết.
+ Tế bào sao (Ito): nằm dưới nội mô, dự trữ vitamin A, và có vai trò trung tâm trong xơ hoá.
I.3. MÔ HỌC GAN – TIỂU THÙY, HỆ THỐNG ỐNG MẬT, HỆ XOANG
1.3.1. Cấu trúc mô học
Đơn vị cơ bản: tiểu thùy gan cổ điển – hình lục giác, ở giữa có tĩnh mạch trung tâm.
Tại mỗi góc của tiểu thùy: tam giác cửa (portal triad) gồm:
+ Nhánh động mạch gan
+ Nhánh tĩnh mạch cửa
+ Ống mật nhỏ
Tất cả được bao quanh bởi mô liên kết.
1.3.2. Tế bào gan (hepatocytes)
Chiếm 70–80% khối lượng gan.
Có nhân lớn, giàu bào quan: lưới nội chất nhẵn – thô, bộ Golgi, ty thể → thực hiện các chức năng chuyển hoá, tổng hợp, phân giải.
Xếp thành bè gan (hepatic plates) chạy hướng tâm từ portal triad đến tĩnh mạch trung tâm.
1.3.3. Hệ thống mật – canaliculus
Tế bào gan bài tiết mật vào các tiểu quản mật (canaliculus) nằm giữa 2 tế bào gan kề nhau.
Dẫn mật vào ống mật gian tiểu thùy → ống mật lớn → ống gan phải – trái → ống gan chung.
I.4. KHÔNG GIAN DẪN TRUYỀN – SINH LÝ ĐỘNG HỌC MÔ GAN
1.4.1. Khoảng Disse
Khoảng nhỏ giữa tế bào nội mô sinusoid và bè gan.
Tại đây có trao đổi chất giữa huyết tương và tế bào gan.
Tế bào sao (stellate cells) nằm trong khoảng Disse – có vai trò trong:
+ Dẫn truyền tín hiệu viêm
+ Dự trữ vitamin A
+ Khi hoạt hoá → tiết collagen → xơ hoá.
1.4.2. Cấu trúc ba trục – portal triad
Động mạch → cung cấp oxy
Tĩnh mạch cửa → chất hấp thu và kháng nguyên
Ống mật → dẫn mật ra ngoài
Các yếu tố này tương tác chặt chẽ → khi một yếu tố rối loạn → ảnh hưởng toàn trục.
I.5. Ý NGHĨA TRONG BỆNH HỌC XƠ GAN
| Yếu tố giải phẫu | Hậu quả trong xơ gan |
|---|---|
| Tĩnh mạch cửa | Tăng áp lực → cổ trướng, giãn tĩnh mạch |
| Sinusoid gan | Bị chèn ép bởi mô xơ → thiếu máu vi mô |
| Khoảng Disse | Collagen tích tụ → mất trao đổi chất |
| Tế bào sao | Hoạt hoá thành myofibroblast → sản xuất mô xơ |
| Tam giác cửa | Bị thay thế bằng sẹo → phá vỡ lưu thông mật – máu |
PHẦN II: SINH LÝ HOẠT ĐỘNG TOÀN DIỆN CỦA GAN (NỀN TẢNG PHÂN TỬ CHO CÁC RỐI LOẠN TRONG XƠ GAN)
2.1. CHUYỂN HÓA GLUCOSE – ĐIỀU HÒA ĐƯỜNG HUYẾT
2.1.1. Tổng hợp và phân giải glycogen (glycogenesis – glycogenolysis)
Sau ăn: insulin kích hoạt glycogen synthase → gan chuyển glucose thành glycogen để dự trữ.
Khi đói: glucagon, adrenaline hoạt hóa glycogen phosphorylase → phân giải glycogen thành glucose → duy trì đường huyết ổn định.
2.1.2. Tân tạo glucose (gluconeogenesis)
Khi nguồn glycogen cạn, gan sử dụng lactate (từ cơ), glycerol (từ mỡ), amino acid (chủ yếu alanin) để tạo glucose.
Các enzyme quan trọng:
+ Pyruvate carboxylase
+ Phosphoenolpyruvate carboxykinase (PEPCK)
+ Fructose-1,6-bisphosphatase
+ Glucose-6-phosphatase (đặc hiệu cho gan)
2.1.3. Ý nghĩa trong xơ gan
Gan xơ mất dần khả năng tân tạo glucose → hạ đường huyết, mệt mỏi sau nhịn đói.
Đề kháng insulin xuất hiện do tăng cytokine viêm → tiểu đường do gan (hepatogenic diabetes).
2..2. CHUYỂN HÓA LIPID – TỔNG HỢP ACID MẬT, CHOLESTEROL VÀ VẬN CHUYỂN MỠ
2.2.1. Tổng hợp cholesterol
Diễn ra từ acetyl-CoA qua con đường mevalonate, xúc tác bởi HMG-CoA reductase – enzyme bị ức chế bởi nhóm thuốc statin.
Cholesterol dùng để:
+ Tạo màng tế bào
+ Tổng hợp hormone steroid
+ Tiền chất acid mật
2.2.2. Tổng hợp và tái tuần hoàn acid mật
Cholesterol chuyển thành acid mật nguyên phát (cholic, chenodeoxycholic) → liên hợp với glycin hoặc taurine → bài tiết vào mật.
95% acid mật được tái hấp thu ở hồi tràng và trở lại gan qua chu trình gan – ruột (enterohepatic).
2.2.3. Vận chuyển lipid
Gan tổng hợp:
+ VLDL: vận chuyển triglyceride
+ LDL: đưa cholesterol tới mô ngoại vi
+ HDL: thu hồi cholesterol về gan
Trong xơ gan: giảm tổng hợp apoprotein → rối loạn mỡ máu, giảm HDL, tăng cholesterol bất thường.
2.3. CHUYỂN HÓA PROTEIN – TỔNG HỢP, GIẢI ĐỘC AMMONIA
2.3.1. Tổng hợp protein huyết tương
Gan tạo ra:
+ Albumin: giữ áp suất keo huyết tương, vận chuyển thuốc, bilirubin.
+ Globulin α, β
+ Yếu tố đông máu: II, VII, IX, X (phụ thuộc vitamin K)
+ Transferrin, ceruloplasmin (vận chuyển sắt, đồng)
+ Protein C – S (chống đông), CRP, IGF-1
2.3.2. Chu trình ure – giải độc NH₃
Ammonia sinh ra từ chuyển hóa protein → độc cho thần kinh trung ương.
Gan chuyển NH₃ thành ure qua chu trình:
+ Carbamoyl phosphate synthetase I (CPS1)
+ Ornithine transcarbamylase
+ Argininosuccinate lyase
2.3.3. Xơ gan gây:
Giảm albumin → phù, cổ trướng.
Giảm yếu tố đông máu → INR ↑, nguy cơ xuất huyết.
Ammonia tăng → não gan (hepatic encephalopathy): lú lẫn, hôn mê.
2.4. CHUYỂN HÓA HEM – BILIRUBIN – CHỨC NĂNG MẬT
2.4.1. Chuyển hóa bilirubin
Hồng cầu già → phá huỷ → hem → biliverdin → bilirubin gián tiếp (tự do).
Gan tiếp nhận bilirubin gián tiếp → liên hợp với glucuronic acid nhờ UDP-glucuronyltransferase → bilirubin trực tiếp (tan trong nước) → bài tiết vào mật.
2.4.2. Chức năng mật
Mật chứa:
+ Acid mật
+ Cholesterol
+ Bilirubin liên hợp
+ Lecithin, bicarbonate
Vai trò:
+ Nhũ hóa chất béo → hấp thu vitamin A, D, E, K.
+ Đào thải cholesterol dư thừa và bilirubin.
2.4.3. Trong xơ gan:
Ứ mật → vàng da, ngứa, phân bạc màu, nước tiểu sậm.
Acid mật trong máu gây viêm mô gan tiến triển.
2.5. CHUYỂN HÓA THUỐC VÀ CHẤT ĐỘC
2.5.1. Giai đoạn I – oxy hóa, khử, thủy phân
Enzyme: Cytochrome P450 (CYP3A4, CYP2C9…)
Biến thuốc tan trong lipid thành chất phân cực hơn.
2.5.2. Giai đoạn II – liên hợp
Gan liên hợp chất đã qua pha I với glucuronate, sulfate, glutathione → giúp đào thải qua thận/mật.
2.5.3. Trong xơ gan:
Giảm khả năng chuyển hóa thuốc → dễ ngộ độc.
Ví dụ:
+ Paracetamol → độc cho gan nếu không chuyển hóa kịp.
+ Diazepam, morphin → kéo dài tác dụng do giảm thanh thải.
2.6. CHỨC NĂNG MIỄN DỊCH – HÀNG RÀO VI SINH
2.6.1. Tế bào Kupffer
Đại thực bào cố định ở sinusoid gan.
Dọn dẹp vi khuẩn, mảnh tế bào chết, phức hợp miễn dịch.
Tiết cytokine điều hòa viêm (IL-1, TNF-α…).
2.6.2. Gan là cơ quan dung nạp miễn dịch đặc biệt
Trình diện kháng nguyên nhưng không kích hoạt mạnh → giữ cân bằng miễn dịch.
Tính chất này lý giải việc gan là cơ quan dễ ghép nhất.
2.6.3. Trong xơ gan:
Giảm Kupffer → nhiễm trùng dễ hơn.
Mất dung nạp → tự miễn gan xảy ra trong một số bệnh (AIH, PBC…).
2.7. CHỨC NĂNG NỘI TIẾT VÀ THẦN KINH
2.7.1. Nội tiết
Chuyển hoá hormone:
+ Estrogen: giảm phân hủy → nữ hóa tuyến vú.
+ Testosterone: giảm tổng hợp → teo tinh hoàn.
+ Aldosterone: giữ muối nước → cổ trướng.
Tổng hợp:
+ IGF-1: kích thích tăng trưởng.
+ TBG: vận chuyển thyroxine.
2.7.2. Thần kinh thực vật
Chi phối bởi:
+ Phó giao cảm (dây X): điều hoà tiết mật.
+ Giao cảm (đám rối tạng): kiểm soát lưu lượng máu.
Trong xơ gan: tăng hoạt giao cảm → co mạch thận, giữ muối nước.
TỔNG KẾT VÀ LIÊN KẾT ĐIỀU TRỊ
| Chức năng sinh lý | Rối loạn khi xơ gan | Gợi ý điều trị |
|---|---|---|
| Tổng hợp protein | Giảm albumin, đông máu | Truyền albumin, vitamin K |
| Giải độc NH₃ | Não gan | Lactulose, rifaximin, BCAA |
| Sản xuất mật | Ngứa, vàng da | Ursodeoxycholic acid, cholestyramine |
| Chuyển hóa thuốc | Ngộ độc thuốc | Giảm liều, chọn thuốc ít chuyển hóa gan |
| Miễn dịch | Nhiễm trùng, viêm gan tự miễn | Kháng sinh, điều hòa miễn dịch |
| Nội tiết | Nữ hóa, giữ nước | Theo dõi hormon, kiểm soát dịch, lợi tiểu |
PHẦN III: CƠ CHẾ SINH HỌC PHÂN TỬ GÂY XƠ GAN (Xây nền lý luận cho chiến lược điều trị – tái cấu trúc mô gan)
3.1. KÍCH HOẠT TẾ BÀO SAO (HEPATIC STELLATE CELLS – HSCs)
3.1.1. Vị trí và trạng thái sinh lý
Tế bào sao nằm trong khoảng Disse, giữa mao mạch xoang gan và bè gan.
Ở trạng thái bình thường:
+ HSCs không phân chia
+ Chức năng: dự trữ vitamin A dưới dạng retinyl ester
+ Duy trì ổn định cấu trúc vi mạch gan
3.1.2. Khi gan bị tổn thương mạn
Tổn thương lặp đi lặp lại bởi:
+ Virus (HBV, HCV)
+ Rượu – acetaldehyde
+ Acid mật tích tụ
+ Lipopolysaccharide từ ruột (trong tăng tính thấm ruột)
+ Cytokine viêm (IL-1β, TNF-α)
→ hoạt hóa tế bào Kupffer, bạch cầu mono, tế bào gan chết → phóng thích TGF-β, PDGF, ROS.
3.1.3. Quá trình hoạt hóa HSCs
Chuyển dạng hình thái từ tế bào không phân chia → myofibroblast (biệt hóa một phần cơ trơn)
Biểu hiện:
+ Tăng α-SMA (alpha smooth muscle actin)
+ Mất hạt lipid chứa vitamin A
+ Tăng khả năng tăng sinh, di chuyển, co kéo
+ Bắt đầu tiết collagen type I, III, laminin, fibronectin → hình thành mô xơ.
3.2. TÍN HIỆU CHỦ YẾU KÍCH HOẠT XƠ HÓA
3.2.1. TGF-β1 (Transforming Growth Factor beta 1)
Là yếu tố xơ hóa mạnh nhất trong sinh học gan.
Tác dụng:
+ Tăng biểu hiện gene mã hóa collagen (COL1A1, COL3A1)
+ Ức chế matrix metalloproteinases (MMPs)
+ Tăng TIMP (tissue inhibitor of metalloproteinase) → ngăn phân giải mô xơ
+ Cảm ứng epithelial-mesenchymal transition (EMT) ở tế bào gan → tạo tế bào giống xơ
3.2.2. PDGF (Platelet-Derived Growth Factor)
Yếu tố tăng trưởng mạnh với HSCs → thúc đẩy tăng sinh, di chuyển.
3.2.3. ROS (Reactive Oxygen Species)
Tạo bởi rượu, viêm, độc tố.
Gây hoại tử tế bào gan, hoạt hóa HSCs thông qua NF-κB, kích thích IL-6, TNF-α.
3.2.4. Angiotensin II và endothelin-1
Gây co mạch, tăng áp lực nội tại trong xoang gan → tăng lực kéo mô xơ
Đồng thời kích hoạt HSCs theo cơ chế “cơ học hóa học”.
3.3. TẠO MÔ XƠ VÀ HÌNH THÀNH SẸO
3.3.1. Collagen và thành phần mô đệm
Bình thường: gan chứa 2–4% collagen, chủ yếu type IV và VI (tại nền mô).
Khi xơ hóa:
+ Collagen type I và III tăng đột biến (gấp 6–10 lần), chiếm tới 30–40% protein mô.
+ Lắng đọng bất thường quanh tĩnh mạch cửa, khoảng Disse, xoang gan → chia cắt mô thành nút tái tạo giả.
3.3.2. Tái tổ chức vi mạch
Sinusoid bị bít kín → mất tính mao mạch hóa đặc trưng.
Tăng tạo mạch máu mới bất thường (angiogenesis) → các mao mạch mới không có chức năng trao đổi.
Hình thành các shunt (nối tắt) trong gan → máu đi nhanh qua mà không trao đổi.
3.3.3. MMPs và TIMPs
Bình thường: MMP-1, MMP-13 phân hủy collagen → cân bằng xơ hóa.
Xơ gan:
+ Tăng TIMP-1, TIMP-2 → ức chế MMP → mô xơ không bị phân giải.
+ Vòng xoắn bệnh lý: càng xơ → càng giảm khả năng sửa chữa.
3.4. GIAI ĐOẠN XƠ – MẤT BÙ – BIẾN CHỨNG
3.4.1. Tiến trình tự nhiên
Giai đoạn đầu: mô xơ bắt đầu bám quanh khoảng cửa, tĩnh mạch trung tâm.
Giai đoạn giữa: collagen lan tỏa, tạo cầu nối → chia cắt gan thành thùy giả.
Giai đoạn cuối: xơ gan mất bù với biến chứng:
+ Cổ trướng
+ Não gan
+ Xuất huyết tiêu hoá
+ Hội chứng gan – thận
+ Ung thư biểu mô tế bào gan (HCC)
3.4.2. Vai trò của vi khuẩn đường ruột
Tăng tính thấm ruột → vi khuẩn, LPS vào máu → kích hoạt TLR4 – NFκB trên Kupffer, HSC → tăng xơ.
Là cơ chế đích cho các thuốc ức chế viêm ruột – gan trục (rifaximin, probiotics…).
3.5. ĐIỂM MỞ CHO LIỆU PHÁP MỚI
| Mục tiêu can thiệp | Hướng tiếp cận |
|---|---|
| TGF-β1 | Chất ức chế TGF-β receptor (galunisertib…) |
| HSC hoạt hóa | Block PDGF, angiotensin II (losartan, telmisartan) |
| ROS – viêm | Chất chống oxy hóa (vitamin E, N-acetylcystein, silymarin) |
| MMP/TIMP | Tăng MMP, giảm TIMP (interferon gamma, gene therapy) |
| Tái cấu trúc | Thuốc kháng tạo mạch (bevacizumab…), ức chế EMT |
KẾT LUẬN PHẦN III
Xơ gan không phải là tích tụ xơ thụ động, mà là một quá trình viêm – tái cấu trúc – phản ứng tế bào chủ động.
Tế bào sao (HSC) đóng vai trò trung tâm, kích hoạt bởi TGF-β, ROS, tín hiệu cơ học – miễn dịch – nội tiết.
Quá trình hình thành sẹo là vòng xoắn bệnh lý giữa:
Tổn thương → viêm → hoạt hoá HSC → tiết collagen → xơ hoá → giảm tuần hoàn → tổn thương thêm.
Kiến thức này mở ra cơ hội điều trị ngay cả khi mô xơ đã hình thành, nếu biết cách chặn tín hiệu – phục hồi MMP – kích hoạt sửa chữa nội tại.
PHẦN IV – GIẢI PHẪU BỆNH VÀ MÔ HỌC CỦA XƠ GAN (Giải mã hình ảnh tổn thương thực thể để đối chiếu lâm sàng – sinh hoá – chẩn đoán mô học)
4.1. CẤU TRÚC TIỂU THÙY GAN BÌNH THƯỜNG
4.1.1. Tiểu thùy cổ điển
Hình lục giác với:
+ Trung tâm: tĩnh mạch trung tâm (central vein)
+ Các góc: bộ ba cửa (portal triads) – gồm nhánh động mạch gan, tĩnh mạch cửa, ống mật
Bè tế bào gan xếp hình nan hoa hướng tâm, xen giữa là mao mạch xoang (sinusoids)
Khoảng Disse: nằm giữa tế bào gan và nội mô sinusoid
4.1.2. Dòng chảy máu và mật
Máu: từ tĩnh mạch cửa và động mạch → sinusoids → tĩnh mạch trung tâm
Mật: từ tế bào gan → tiểu quản mật → ống mật vùng cửa (ngược chiều dòng máu)
4.2. BIẾN ĐỔI MÔ HỌC TRONG XƠ GAN
4.2.1. Hình thành vách xơ (fibrous septa)
Sự hoạt hóa tế bào sao tạo dải mô xơ nối các tiểu thùy → phân cắt mô gan → mất cấu trúc hình lục giác
Collagen type I và III thay thế mô mềm → gan cứng
4.2.2. Xuất hiện tiểu thùy giả (pseudolobules)
Các “nút” tế bào gan còn lại bị bao quanh bởi vách xơ → hình thành nút tái sinh (regenerative nodules)
Không còn tĩnh mạch trung tâm → rối loạn tuần hoàn máu vi mô
Không theo định hướng giải phẫu ban đầu → suy giảm chức năng toàn hệ
4.2.3. Tái cấu trúc xoang gan
Mao mạch xoang bị xơ hoá, mất cấu trúc fenestrae → gọi là capillarization of sinusoids
Tế bào nội mô bị biến đổi → giảm trao đổi chất giữa máu và tế bào gan
Tắc nghẽn vi mạch → thiếu oxy mô → tế bào gan thoái hóa
4.3. BIẾN ĐỔI CỦA TẾ BÀO GAN
4.3.1. Thoái hóa và hoại tử
Tế bào gan có thể:
+ Thoái hoá mỡ (steatosis): bào tương chứa không bào mỡ lớn
+ Thoái hoá nước (hydropic degeneration): sưng tế bào, nhân nhạt màu
+ Hoại tử đông (co rút, vỡ nhân) trong viêm cấp
+ Hoại tử điểm hoặc hoại tử cầu nối (bridging necrosis) trong tổn thương mạn
4.3.2. Tăng sinh và dị dạng hạt nhân
Nút tái sinh thường chứa tế bào gan với nhân dị hình, đa nhân, tăng tỷ lệ nhân/bào tương.
Có thể khó phân biệt với ung thư tế bào gan (HCC) nếu không có phân tích chuyên sâu
4.3.3. Tế bào Kupffer và miễn dịch
Tăng hoạt trong viêm – xơ → tăng bắt hồng cầu già, tăng tiết cytokine
Xơ gan lâu ngày: giảm dần số lượng, đặc biệt nếu có tắc nghẽn sinusoid
4.4. BIẾN ĐỔI ỐNG MẬT – MẠCH MÁU – MÔ LIÊN KẾT
4.4.1. Tân tạo ống mật (ductular reaction)
Vùng cửa xuất hiện các ống mật nhỏ mới sinh, chạy trong mô xơ
Đây là phản ứng đặc trưng trong xơ mật nguyên phát (PBC), viêm ống mật xơ hóa nguyên phát (PSC)
4.4.2. Bất thường mạch máu
Các shunt (nối tắt) hình thành giữa tĩnh mạch cửa và gan – hoặc giữa gan và hệ tĩnh mạch chủ
Mạch máu tân sinh không đúng định hướng → máu chảy qua gan nhanh nhưng không hiệu quả
4.4.5. PHÂN LOẠI MÔ HỌC XƠ GAN
| Loại xơ gan | Đặc điểm mô học |
|---|---|
| Xơ gan vi thể (micronodular) | Nút <3 mm, thường do rượu |
| Xơ gan đại thể (macronodular) | Nút >3 mm, không đều, do HBV, HCV |
| Xơ gan hỗn hợp | Gồm cả micronodule và macronodule |
4.6. ĐẶC ĐIỂM MÔ HỌC GIÚP PHÂN BIỆT VỚI UNG THƯ GAN
| Tiêu chí | Nút tái sinh | HCC |
|---|---|---|
| Bao xơ | Có | Có hoặc không |
| Kiến trúc bè | Dưới 2 lớp tế bào | >3 lớp, bè dày |
| Mạch máu | Không tân tạo mạnh | Tân tạo động mạch nội nốt |
| Nhân | Bình thường hoặc dị hình nhẹ | Dị dạng rõ, phân bào cao |
| CD34 | Âm tính (hoặc thấp) | Tăng mạnh (dấu hiệu capillarization) |
4.7. SINH THIẾT GAN – VAI TRÒ CHẨN ĐOÁN
Sinh thiết mô gan vẫn là tiêu chuẩn vàng để xác định:
+ Mức độ xơ (Fibrosis staging)
+ Hoạt tính viêm (Activity grade)
+ Nguyên nhân: nhiễm mỡ, viêm ống mật, viêm gan tự miễn, lắng đọng đồng/sắt…
Một số thang điểm mô học:
+ METAVIR (F0–F4)
+ Ishak (0–6)
+ Batts–Ludwig
4.8. MÔ HỌC VÀ LÂM SÀNG: MỐI LIÊN HỆ CỐT LÕI
| Mô học | Hậu quả chức năng |
|---|---|
| Collagen quanh sinusoid | Tăng kháng dòng máu → tăng áp cửa |
| Tái cấu trúc tiểu thùy | Mất điều hòa chuyển hóa, giảm oxy |
| Tân tạo ống mật | Ứ mật, ngứa da |
| Viêm kéo dài | Hoại tử tế bào gan, mệt mỏi, tăng men gan |
| Shunt mạch máu | Não gan, tăng nguy cơ nhiễm trùng |
PHẦN V – SINH LÝ BỆNH HỌC CỦA XƠ GAN (Cơ chế gây biến chứng – cách gan chuyển từ tổn thương đến sụp đổ chức năng)
5.1. TỔNG QUAN SINH LÝ BỆNH
Xơ gan không chỉ là hiện tượng “xơ hóa” mô gan mà là một hội chứng tiến triển đa hệ thống, với:
+ Rối loạn cấu trúc vi mạch → tăng áp tĩnh mạch cửa
+ Rối loạn chức năng tế bào gan → giảm chuyển hoá – giải độc – tổng hợp
+ Rối loạn miễn dịch – nội tiết → nhiễm trùng – phù – hội chứng gan–thận
Kết quả là: một vòng xoắn bệnh lý, với gan mất bù, các cơ quan khác bị kéo theo suy sụp (thận, não, ruột, tuần hoàn…).
5.2. TĂNG ÁP TĨNH MẠCH CỬA (PORTAL HYPERTENSION)
5.2.1. Cơ chế
Bình thường: áp lực tĩnh mạch cửa ~5 mmHg.
Khi vượt 10–12 mmHg: xuất hiện giãn tĩnh mạch thực quản, lách to, cổ trướng.
Nguyên nhân chính:
+ Cản trở dòng máu qua gan do mô xơ
+ Tăng trương lực mạch máu nội tại do endothelin-1, thiếu nitric oxide
+ Tân tạo mạch máu bất thường, mất tổ chức mao mạch xoang
5.2.2. Hậu quả
| Biến chứng | Cơ chế |
|---|---|
| Giãn tĩnh mạch thực quản | Tăng dòng máu phụ qua hệ nối cửa – chủ |
| Xuất huyết tiêu hoá | Vỡ giãn tĩnh mạch do áp cao |
| Lách to, giảm tiểu cầu | Ứ máu tĩnh mạch lách |
| Cổ trướng | Tăng áp cửa + giảm albumin máu |
5.3. CỔ TRƯỚNG (ASCITES)
5.3.1. Cơ chế
Tăng áp lực thủy tĩnh trong hệ cửa → đẩy dịch ra khoang màng bụng
Giảm albumin máu → giảm áp lực keo → dịch thoát ra nhiều hơn
Tăng aldosterone và ADH thứ phát → giữ muối nước, làm nặng cổ trướng
5.3.2. Hệ quả
Gây khó thở, chán ăn, đau bụng mơ hồ
Dễ nhiễm trùng dịch báng (SBP – spontaneous bacterial peritonitis)
5.4. NÃO GAN (HEPATIC ENCEPHALOPATHY)
5.4.1. Cơ chế
Ammonia (NH₃) sinh ra từ ruột → không được gan chuyển thành ure → tích tụ
Đi qua hàng rào máu–não → gây phù não, rối loạn dẫn truyền thần kinh (GABAergic)
Yếu tố thúc đẩy: xuất huyết tiêu hoá, táo bón, nhiễm trùng, tăng protein khẩu phần
5.4.2. Biểu hiện lâm sàng
Từ rối loạn nhẹ: mất ngủ, giảm tập trung
Đến nặng: run vẫy cánh, lú lẫn, hôn mê
5.5. HỘI CHỨNG GAN – THẬN (HEPATORRENAL SYNDROME – HRS)
5.5.1. Cơ chế
Tăng hoạt giao cảm → co mạch thận → giảm tưới máu thận
Kèm theo giãn mạch toàn thân do NO, glucagon → tụt thể tích tuần hoàn hiệu dụng
Cầu thận không được tổn thương thực thể, nhưng mất khả năng lọc → suy thận chức năng
5.5.2. Đặc điểm
Creatinine tăng dần, không đáp ứng với bù dịch
Không tiểu máu, không protein niệu
Phân biệt với hoại tử ống thận cấp (ATN)
5.6. UNG THƯ BIỂU MÔ TẾ BÀO GAN (HEPATOCELLULAR CARCINOMA – HCC)
5.6.1. Cơ chế
Nút tái sinh lặp đi lặp lại → tăng phân bào, tăng đột biến
TGF-β, VEGF, β-catenin, p53… bị đột biến → mất kiểm soát tăng sinh
HCC thường phát sinh trên nền xơ gan mạn tính (80–90% trường hợp)
5.6.2. Dấu hiệu
Đau âm ỉ hạ sườn phải
Tăng alpha-fetoprotein (AFP)
Khối u tăng ngấm thuốc trong thì động mạch, rửa nhanh thì tĩnh mạch trên CT/MRI
5.7. HỘI CHỨNG GAN – PHỔI (HEPATOPULMONARY SYNDROME)
Xơ gan → tăng NO và prostaglandin → giãn mạch phổi lan toả
Hậu quả: mất cân bằng thông khí – tưới máu (V/Q mismatch)
Biểu hiện: khó thở tăng khi đứng (orthodeoxia), tím môi, PaO₂ < 80 mmHg
5.8. SUY KIỆT – RỐI LOẠN NỘI TIẾT
| Biến đổi | Giải thích |
|---|---|
| Teo cơ – suy kiệt | Rối loạn chuyển hoá protein, kháng insulin, giảm IGF-1 |
| Nữ hoá tuyến vú, giảm libido | Tăng estrogen do giảm chuyển hoá |
| Loãng xương | Giảm vitamin D, IGF-1, tăng IL-6 |
TỔNG KẾT PHẦN V
Xơ gan gây rối loạn hệ thống qua 5 trục chính:
- Tuần hoàn cửa → giãn tĩnh mạch, xuất huyết
- Áp lực thẩm thấu → cổ trướng, phù
- Thải độc thần kinh → não gan
- Huyết động thận → hội chứng gan–thận
- Tăng sinh không kiểm soát → HCC
→ Các cơ chế này là nền tảng để xây dựng nguyên lý điều trị theo hướng chặn vòng xoắn bệnh lý, phục hồi chức năng, tái thông dòng chảy vi mạch và hỗ trợ tế bào gan còn sống sót.
PHẦN VI – CƠ SỞ HOÁ SINH ỨNG DỤNG TRONG CHẨN ĐOÁN & ĐIỀU TRỊ XƠ GAN (Diễn giải các xét nghiệm huyết học – sinh hoá – đông máu để định hướng lâm sàng và tiên lượng)
6.1. NHÓM XÉT NGHIỆM CHỨC NĂNG GAN CƠ BẢN
6.1.1. Men gan (Transaminase – AST, ALT)
AST (Aspartate aminotransferase): chủ yếu từ ty thể → tăng nhiều khi tổn thương tế bào nặng (rượu, viêm cấp).
ALT (Alanine aminotransferase): đặc hiệu hơn cho tế bào gan, tăng trong viêm gan virus, nhiễm độc.
Ý nghĩa trong xơ gan:Giai đoạn đầu: AST, ALT tăng nhẹ → do viêm mạn tính.
Giai đoạn cuối: AST, ALT giảm dần do tế bào gan mất khả năng hoạt động → men thấp không đồng nghĩa nhẹ.
6.1.2. Phosphatase kiềm (ALP) và GGT
ALP: tăng mạnh trong ứ mật, tắc mật trong/ngoài gan.
GGT (gamma-glutamyltransferase): tăng song hành với ALP → loại trừ tăng ALP do xương.
6.1.3. Bilirubin toàn phần – trực tiếp – gián tiếp
Tăng trong:
+ Tổn thương tế bào gan (giảm liên hợp)
+ Tắc mật (giảm bài tiết mật)
Bilirubin trực tiếp tăng ưu thế → nghi tắc mật.
Gián tiếp tăng ưu thế → viêm gan, tan máu, bệnh Gilbert.
6.2. CHỨC NĂNG TỔNG HỢP CỦA GAN
6.2.1. Albumin
Do gan tổng hợp độc quyền.
Vai trò:
+ Duy trì áp lực keo
+ Vận chuyển acid béo, thuốc, hormon
Trong xơ gan:
+ Albumin giảm dần → gây phù, cổ trướng, tăng thuốc tự do trong máu.
+ Giá trị < 28 g/L là dấu hiệu xơ gan nặng.
6.2.2. INR và thời gian prothrombin (PT)
Gan tạo ra các yếu tố đông máu (II, VII, IX, X), phụ thuộc vitamin K.
Xơ gan làm giảm tổng hợp → INR ↑, PT kéo dài.
INR là một trong 3 chỉ số đánh giá Child–Pugh và tính điểm MELD.
6.3. CHỨC NĂNG GIẢI ĐỘC
6.3.1. Ammonia (NH₃) máu
NH₃ tăng → nguy cơ não gan.
Giá trị bình thường: <50 μmol/L; >100 μmol/L cần xử lý tích cực.
Lưu ý: NH₃ dễ nhiễm sai số do thời gian bảo quản, lấy máu tĩnh mạch hay động mạch.
6.3.2. Lactate
Gan chuyển hoá lactate → pyruvate → glucose.
Xơ gan nặng → tăng lactate máu → nhiễm toan acid lactic type B (thường gặp khi sốc, nhiễm trùng).
6.4. XÉT NGHIỆM VỀ BIẾN CHỨNG – PHỤ
6.4.1. Công thức máu
| Thông số | Biến đổi thường gặp trong xơ gan |
|---|---|
| Hồng cầu | Giảm do thiếu B12/folate, xuất huyết |
| Bạch cầu | Giảm do lách to, ức chế tuỷ xương |
| Tiểu cầu | Giảm rất sớm do tăng bắt giữ tại lách, giảm thrombopoietin |
6.4.2. Điện giải đồ
Giảm Na⁺ (hyponatremia pha loãng) do tăng ADH thứ phát.
K⁺: có thể giảm (do lợi tiểu) hoặc tăng (suy thận, dùng spironolactone).
6.4.3. BUN – Creatinine
BUN giảm (do gan giảm tổng hợp ure).
Creatinine thường thấp giả tạo (do giảm khối cơ), nhưng khi tăng → dấu hiệu rất nghiêm trọng (HRS).
6.5. CÁC CHỈ SỐ ĐÁNH GIÁ MỨC ĐỘ XƠ GAN & TIÊN LƯỢNG
6.5.1. Child–Pugh score
| Tiêu chí | Thang điểm |
|---|---|
| Bilirubin | <2 mg/dL (1), 2–3 (2), >3 (3) |
| Albumin | >3.5 g/dL (1), 2.8–3.5 (2), <2.8 (3) |
| INR | <1.7 (1), 1.7–2.3 (2), >2.3 (3) |
| Cổ trướng | Không (1), nhẹ (2), kháng trị (3) |
| Não gan | Không (1), độ I–II (2), độ III–IV (3) |
A: 5–6 điểm (xơ còn bù)
B: 7–9 điểm
C: 10–15 điểm (xơ mất bù)
6.5.2. MELD score (Model for End-stage Liver Disease)
Công thức (MELD-Na):
MELD = 3.78 × ln(bilirubin) + 11.2 × ln(INR) + 9.57 × ln(creatinine) + 6.43 – Na factor
Dự báo sống còn trong 3 tháng:
+ MELD > 15: cân nhắc ghép gan
+ MELD > 30: nguy cơ tử vong rất cao
6.6. DẤU HIỆU ĐẶC BIỆT TRONG PHÂN BIỆT NGUYÊN NHÂN
| Nguyên nhân | Dấu hiệu hoá sinh |
|---|---|
| Viêm gan virus | ALT/AST ↑↑, tỷ lệ ALT/AST >1 |
| Rượu | AST/ALT >2, GGT ↑, ferritin ↑ |
| Gan nhiễm mỡ | ALT > AST, triglyceride ↑ |
| PBC | ALP ↑ rất cao, AMA dương tính |
| Hemochromatosis | Ferritin ↑, Transferrin sat >45% |
| Wilson | Ceruloplasmin ↓, đồng niệu 24h ↑ |
| Autoimmune | ALT ↑, ANA +, IgG ↑ |
6.7. ỨNG DỤNG TRONG THEO DÕI ĐIỀU TRỊ
| Xét nghiệm | Theo dõi điều gì |
|---|---|
| Albumin | Hiệu quả bổ sung dinh dưỡng, tiên lượng |
| INR | Nguy cơ xuất huyết, đáp ứng vitamin K |
| Bilirubin | Theo dõi tiến triển tắc mật hoặc chết tế bào gan |
| NH₃ | Hiệu quả điều trị não gan |
| Creatinine | Diễn biến hội chứng gan–thận |
KẾT LUẬN PHẦN VI
Các xét nghiệm hoá sinh không đơn thuần là con số, mà là chỉ dấu phân tử phản ánh:
Mức độ tổn thương – viêm – sửa chữa
Khả năng tổng hợp – giải độc – chuyển hóa
Nguy cơ biến chứng và tử vong
Chúng giúp xác lập nguyên lý:
Khi nào cần can thiệp?
Cần theo dõi gì?
Ai cần được ghép gan?
PHẦN VII – NGUYÊN LÝ ĐIỀU TRỊ TOÀN DIỆN BỆNH XƠ GAN(Tổng hợp giải phẫu – sinh lý – hoá sinh thành hệ điều trị có cơ sở khoa học)
7.1. TRIẾT LÝ CỐT LÕI: KHÔNG CHỈ CHỮA MỘT CƠ QUAN
Xơ gan không chỉ là bệnh của riêng gan, mà là bệnh hệ thống, gây:
Rối loạn huyết động (gan – thận – não)
Suy dinh dưỡng – miễn dịch
Viêm mạn – sẹo hoá – tăng sinh không kiểm soát
Do đó, nguyên lý điều trị phải hướng đến:
Ngăn vòng xoắn xơ hoá – viêm – suy
Bảo toàn – phục hồi – thay thế chức năng
Điều trị nguyên nhân gốc + hỗ trợ đa hệ
7.2. NGUYÊN LÝ 1 – KIỂM SOÁT NGUYÊN NHÂN TỔN THƯƠNG
| Nguyên nhân | Hành động |
|---|---|
| Viêm gan B/C | Thuốc kháng virus (tenofovir, entecavir, sofosbuvir…) |
| Rượu | Cai rượu tuyệt đối, hỗ trợ dinh dưỡng, tâm lý |
| NAFLD/NASH | Giảm cân, điều trị đề kháng insulin (pioglitazone, GLP-1 RA) |
| Wilson | Chelator đồng (penicillamine, trientine), bổ sung kẽm |
| Tự miễn | Corticoid ± azathioprine, theo dõi kháng thể |
🎯 Mục tiêu: chặn đứng tổn thương mới – giữ phần gan còn lại hoạt động
7.3. NGUYÊN LÝ 2 – ỨC CHẾ VIÊM – CHỐNG XƠ HOÁ – BẢO VỆ MẠCH GAN
7.3.1. Điều chỉnh viêm
Chống viêm nhẹ bằng:
+ Vitamin E, silymarin, curcumin (ức chế NF-κB, ROS)
+ Kẽm: chống peroxid hóa màng
Corticoid: chỉ dùng trong viêm gan tự miễn, hoặc viêm gan rượu nặng có Maddrey >32
7.3.2. Chống xơ hoá và tái cấu trúc
Nghiên cứu mới:
+ Pirfenidone: ức chế TGF-β
+ Losartan: ức chế angiotensin II → giảm hoạt hóa HSC
+ SGLT2i, GLP-1 RA: giảm tiến triển xơ ở NASH
Tăng MMPs: interferon-γ (nghiên cứu), ức chế TIMP
🎯 Mục tiêu: làm chậm quá trình tạo mô xơ – giảm co kéo mạch máu – giữ mô gan mềm, giàu máu
7.4. NGUYÊN LÝ 3 – GIẢI ĐỘC – TĂNG CHUYỂN HOÁ – NUÔI GAN CÒN LẠI
7.4.1. Giải độc NH₃
Lactulose: tạo môi trường acid ruột → giữ NH₄⁺
Rifaximin: giảm vi khuẩn sinh NH₃
BCAA: phục hồi chuyển hoá thần kinh, tăng sử dụng NH₃ ngoại gan
7.4.2. Bổ sung chuyển hoá
Albumin truyền tĩnh mạch (cổ trướng kháng trị, nhiễm trùng)
Bổ sung B1, B6, folate, kẽm
Sữa công thức giàu BCAA (Hepasyn, Hepanat…)
🎯 Mục tiêu: giảm độc tố thần kinh, nuôi dưỡng tế bào gan sống sót, tăng sức tổng hợp
7.5. NGUYÊN LÝ 4 – KIỂM SOÁT HUYẾT ĐỘNG VÀ ÁP LỰC CỬA
7.5.1. Giảm áp lực cửa
Propranolol / Nadolol: giảm dòng máu tĩnh mạch cửa
EVL (thắt tĩnh mạch thực quản) định kỳ
TIPS (shunt cửa–chủ): chỉ định nếu giãn tĩnh mạch nặng, cổ trướng kháng trị
7.5.2. Cân bằng nội môi dịch
Lợi tiểu: spironolactone ± furosemide
Hạn chế muối: <2g/ngày
Chọc tháo dịch cổ trướng lớn → bù albumin
🎯 Mục tiêu: giảm nguy cơ xuất huyết tiêu hoá, cổ trướng, hội chứng gan–thận
7.6. NGUYÊN LÝ 5 – DỰ PHÒNG BIẾN CHỨNG & CHĂM SÓC TỔNG THỂ
| Biến chứng | Phòng & xử lý |
|---|---|
| SBP | Albumin + kháng sinh sớm (cefotaxim, norfloxacin dự phòng) |
| Não gan | Lactulose, rifaximin, hạn chế đạm lúc cấp |
| HCC | Siêu âm + AFP mỗi 6 tháng |
| Xuất huyết tiêu hoá | Propranolol, EVL, omeprazol |
| Suy thận | Theo dõi creatinine, tránh NSAIDs, chỉ dùng lợi tiểu đúng liều |
🎯 Mục tiêu: kiểm soát từng biến chứng trước khi nó gây tử vong
7.7. NGUYÊN LÝ 6 – GHÉP GAN VÀ CHĂM SÓC CUỐI
7.7.1. Ghép gan
Chỉ định khi:
+ MELD ≥15
+ Xơ gan mất bù không phục hồi
+ HCC trong tiêu chuẩn Milan
Sau ghép: sống >10 năm ~80%
Cần đánh giá: tim mạch, tâm thần, hỗ trợ gia đình
7.7.2. Chăm sóc cuối đời
Xơ gan mất bù không hồi phục, biến chứng không kiểm soát
Cần chăm sóc giảm nhẹ: kiểm soát đau, ngứa, phù, suy dinh dưỡng
🎯 Mục tiêu: kéo dài chất lượng sống tối đa – giảm đau đớn cuối đời
7.8. NGUYÊN TẮC LỒNG GHÉP ĐA TẦNG
| Tầng | Biện pháp |
|---|---|
| Cơ chế bệnh học | Chặn TGF-β, giảm ROS, chống xơ hoá |
| Sinh lý gan | Hồi phục trao đổi NH₃, BCAA, lipid |
| Huyết động | Giảm áp cửa, điều hòa mạch thận |
| Hệ thống | Dinh dưỡng – miễn dịch – thần kinh |
| Tương lai | Ghép gan, tế bào gốc, sinh học phân tử |
KẾT LUẬN TOÀN PHẦN
Không có đơn thuốc đơn độc nào chữa khỏi xơ gan – điều trị là một chiến lược:
+ Bắt đầu từ hiểu đúng cơ chế
+ Can thiệp sớm khi chưa mất bù
+ Chống xơ – chống viêm – phục hồi dòng máu
+ Hướng tới giữ gan sống, kiểm soát biến chứng, chuẩn bị ghép nếu cần
CÁC HỢP CHẤT SINH HỌC THỰC VẬT CÓ TIỀM NĂNG ĐIỀU TRỊ XƠ GAN
Danh sách các hợp chất sinh học thực vật (phytochemicals) có tiềm năng điều trị xơ gan, dựa trên cơ chế phân tử đã nghiên cứu trong y học hiện đại. Mỗi nhóm hợp chất được chọn vì khả năng:
Ức chế xơ hoá (anti-fibrotic)
Chống viêm mạn tính (anti-inflammatory)
Kháng oxy hoá mạnh (antioxidant)
Bảo vệ tế bào gan (hepatoprotective)
Ức chế TGF-β, ROS, NF-κB, HSCs…
1. FLAVONOID – POLYPHENOL: CHỐNG OXY HOÁ – GIẢM XƠ
| Hợp chất | Nguồn gốc | Cơ chế chính |
|---|---|---|
| Silymarin | Hạt cây kế sữa (Silybum marianum) | Chống ROS, giảm TGF-β1, ức chế HSC |
| Curcumin | Nghệ (Curcuma longa) | Giảm NF-κB, TGF-β1, chống viêm gan – ức chế xơ |
| Quercetin | Hành tây, táo, vỏ cây | Ức chế collagen I/III, giảm lipid peroxidation |
| Resveratrol | Vỏ nho đỏ, dâu tằm | Tăng SIRT1, giảm viêm, tăng apoptosis HSC |
| Baicalin | Hoàng cầm (Scutellaria baicalensis) | Ức chế NF-κB, giảm fibrogenesis |
| Luteolin | Cần tây, cúc hoa vàng | Ngăn hoạt hoá HSC, giảm α-SMA |
| Apigenin | Rau mùi tây, cúc dại | Chống viêm, giảm TNF-α, TGF-β |
2. TERPENOID – STEROL: CHỐNG XƠ – ỔN ĐỊNH MÀNG
| Hợp chất | Nguồn gốc | Tác dụng |
|---|---|---|
| Glycyrrhizin | Cam thảo (Glycyrrhiza glabra) | Ức chế viêm gan B, giảm ALT, chống xơ |
| Andrographolide | Xuyên tâm liên (Andrographis paniculata) | Giảm TGF-β, tăng IL-10, chống tăng sinh HSC |
| Ursolic acid | Táo xanh, húng tây, loài thảo dược | Giảm α-SMA, collagen I, tăng apoptosis HSC |
| Ginsenosides | Nhân sâm (Panax ginseng) | Điều hoà miễn dịch, chống xơ trên chuột |
| Astragaloside IV | Hoàng kỳ (Astragalus membranaceus) | Ức chế TLR4/NF-κB, tăng tái sinh gan |
3. ALKALOID – CHẤT KHÁNG VIÊM MẠNH
| Hợp chất | Cây thuốc | Tác dụng chính |
|---|---|---|
| Berberine | Hoàng liên, hoàng bá | Ức chế NF-κB, giảm men gan, chống TGF-β1 |
| Oxymatrine | Khổ sâm (Sophora flavescens) | Ức chế collagen I, TGF-β/Smad |
| Tetrandrine | Vỏ cây xuyên bối mẫu (Stephania) | Ức chế tăng sinh HSC, chống co mạch |
| Ligustrazine | Xuyên khung (Ligusticum wallichii) | Tăng lưu thông gan, giảm xơ hoá trên động vật |
4. SAPONIN – CÁC TÁC NHÂN CHỐNG XƠ MẠNH
| Hợp chất | Nguồn | Cơ chế |
|---|---|---|
| Saikosaponin D | Bắc sài hồ (Bupleurum chinense) | Giảm collagen, ức chế viêm |
| Dioscin | Củ mài, thiên ma | Chống tăng sinh HSC, chống oxy hoá |
| Gypenoside | Giảo cổ lam (Gynostemma pentaphyllum) | Tăng apoptosis HSC, điều hoà AMPK/SIRT1 |
5. CÁC NHÓM KHÁC ĐÁNG CHÚ Ý
| Hợp chất | Ghi chú |
|---|---|
| Honokiol | Hậu phác: ức chế TGF-β, ROS, giảm α-SMA |
| Schisandrin B | Ngũ vị tử: tăng GSH gan, tăng ATP, giảm hoại tử |
| Diallyl sulfide | Tỏi: chống độc gan do rượu, kháng viêm |
| β-sitosterol | Có trong mè đen, lúa mạch: ổn định màng, giảm men gan |
CƠ CHẾ ĐÍCH CHUNG CỦA CÁC HỢP CHẤT NÀY
| Đích tác dụng | Hợp chất ảnh hưởng |
|---|---|
| TGF-β/Smad | Curcumin, baicalin, oxymatrine, ginsenosides |
| NF-κB/IL-6/TNF-α | Quercetin, resveratrol, berberine |
| HSCs (tăng sinh, α-SMA) | Apigenin, ursolic acid, saikosaponin D |
| ROS/oxidative stress | Silymarin, schisandrin B, luteolin, honokiol |
| MMP/TIMP | Glycyrrhizin, astragaloside, gypenosides |
GỢI Ý ỨNG DỤNG
- Cấp cứu – kháng viêm – chống độc: silymarin, glycyrrhizin, berberine
- Tái cấu trúc – chống xơ: curcumin, ginsenoside, andrographolide
- Chăm sóc kéo dài: resveratrol, quercetin, baicalin, ursolic acid
- Phối hợp cổ truyền: ngũ vị tử, hoàng kỳ, sài hồ, cam thảo
- Bổ gan – nuôi gan: BCAA + thảo dược chống oxy hóa trên
Biên soạn & biên tập: Bác sĩ Hoàng Đôn Hoà.